HIV-1의 외피에 존재하는 당단백질은 바이러스가 적절한 숙주세포에 부착하여 침투하는 데 필수적이다. HIV의 기능적 당단백질에 단단히 달라붙는 항체는 바이러스의 감염력을 중화시켜 HIV 감염을 예방할 수 있다. HIV는 이러한 항체에 대응하여 다양한 방어 메커니즘을 진화시켰는데, 그중에서 대표적인 것은 「당단백질의 아미노산 시퀀스를 변화」시키거나 「당단백질의 취약한 부분을 글리칸이라는 당으로 은폐」하는 것이다. 이러한 메커니즘들은 바이러스가 항체의 공격을 회피하는 데 효과적이지만, 당단백질은 여전히 결정적인 취약점을 갖고 있다. 왜냐하면 HIV가 감염력을 유지하기 위해서는 당단백질의 특정 부분이 일정하게 보존됨과 동시에 외부로 노출될 필요가 있기 때문이다.
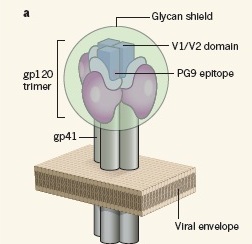
McLellan 등은 Nature 12월 15일호에 기고한 논문에서, "HIV의 표면 당단백질(gp120)과 결합한 PG9이라는 단클론항체의 원자구조를 해명함으로써, gp120의 새로운 약점을 찾아내는 데 성공했다"고 발표하였다. PG9은 광범위한 HIV종을 강력하게 중화시키기 때문에, 그 에피토프(gp120에 결합하는 정확한 부위)는 백신 개발자들의 특별한 관심을 끌어 왔다. 이 에피토프는 V1/V2 도메인이라는 고도의 가변적인 구조 안에 존재하는데, 이 도메인은 글리칸에 의해 은폐되는 것이 보통이며, 모자(cap) 모양의 구조를 형성하여 3개의 gp120 분자를 한데 모아 삼합체(trimer)로 만든다. 이렇게 형성된 gp120의 삼함체는 제 2의 외피 당단백질인 gp41의 삼합체와 결합하게 된다(첨부그림 1a 참조).
McLellan 등은 PG9와 결합하는 V1/V2 도메인의 정확한 위치(에피토프)를 알아내기 위해 이번 연구를 시작하였다. 그러나 PG9이 항원과 결합한 복합체의 구조를 해명하는 것은 간단한 일이 아니었다. 왜냐하면 완전한 항원항체 결합은 세포막에 고정된 온전한 당단백질에 의해 이루어지는 만큼, 에피토프의 존재는 gp120의 4차원적 접힘구조(quaternary folding)에 의존하기 때문이다. 그들은 이에 대한 대안으로 분자 모델링 기법을 이용하여 최소한의 항원 모사체(minimal antigenic mimic)를 구성하였다. 이 모사체는 에피토프의 핵심적인 특징만을 보유한 최소한의 모델로, 네 가닥의 펩타이드로 이루어진 미니 도메인 안에서 하나의 펩타이드 가닥 양쪽에 2개의 글리칸이 배치된 구조를 지니고 있었다.
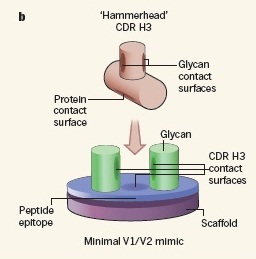
PG9과 PG16(PG9과 매우 유사한 항체)은 하나의 항원결합부위(ABS)에 의해 지배되는 독특한 구조를 갖고 있는데, 이 ABS는 중쇄(heavy chain) 부분에 CDR H3라는 확장된 영역을 포함하고 있다. [CDR H3는 망치머리(hammerhead)와 모양의 독특한 구조를 지니고 있다.] McLellan 등은 이번 연구에서, "가늘고 길다란 모양의 CDR H3가 형태적 장점을 최대한 활용하여, gp120에 있는 2개의 글리칸 사이로 비집고 들어간다"는 사실을 발견하였다. 글리칸 사이로 들어가는 데 성공한 CDR H3는 양 측면에서 글리칸과 접촉함과 동시에 협곡(글리칸 사이의 좁은 공간) 밑바닥의 단백질 표면에 결합하는 것으로 밝혀졌다(첨부그림 1b 참조).
"gp120의 V1/V2 도메인은 변화무쌍하기로 악명이 높은데, PG9은 아미노산 측쇄보다는 단백질의 원자골격에 직접 결합함으로써 V1/V2 도메인의 가변성을 극복하는 것으로 밝혀졌다. 이는` 2개의 글리칸이 진화적으로 보존되어 있다`는 사실과 함께, PG9으로 하여금 HIV-1 변종의 약 80%를 인식하게 하는 데 기여하는 중요한 요인인 것으로 보인다. 이는 면역계가 바이러스의 약점을 공략함으로써 바이러스의 방어망(글리칸)을 궤멸시키는 대표적 사례이다"라고 McLellan 등은 말했다. PG9는 다양한 종의 HIV-1에 대해 강력한 효능을 발휘하는 광범위 중화항체(broadly neutralizing antibody)로 알려져 있지만, 그것이 어떠한 메커니즘을 통하여 HIV-1을 무력화시키는지는 지금껏 명확하게 밝혀지지 않았다. 이번 연구는 PG9이 HIV-1의 당단백질에 결합하는 과정을 규명하고 HIV-1의 약점을 발견함으로써, 효과적인 HIV 백신을 개발하는 데 기여할 것으로 보인다.
출처: 경기과학기술진흥원
자료출처: nature.com
